Ordem de eletronegatividade
2 participantes
Página 1 de 1
 Ordem de eletronegatividade
Ordem de eletronegatividade
Eletronegatividade é a tendência de um elemento de atrair pares eletrônicos ligantes para si em uma ligação química (ou, simplesmente, a tendência a atrair elétrons). Sabe-se que a seguinte lista determina a eletronegatividade de alguns dos principais elementos, em ordem decrescente:
F, O, N, Cl, Br, I, S, C, P, H.
Sei que a eletronegatividade depende do raio atômico (quanto menor o raio atômico, maior a eletronegatividade). Entretanto, como assimilo a lista citada sem precisar de decorebas ou dos raios atômicos dos elementos em questão ? Conheço as "setas" que indicam o sentido de crescimento da eletronegatividade nos elementos da tabela periódica, mas elas não me ajudaram muito a entender.
F, O, N, Cl, Br, I, S, C, P, H.
Sei que a eletronegatividade depende do raio atômico (quanto menor o raio atômico, maior a eletronegatividade). Entretanto, como assimilo a lista citada sem precisar de decorebas ou dos raios atômicos dos elementos em questão ? Conheço as "setas" que indicam o sentido de crescimento da eletronegatividade nos elementos da tabela periódica, mas elas não me ajudaram muito a entender.
miguelito3,1415926- Iniciante
- Mensagens : 5
Data de inscrição : 03/04/2024
 Re: Ordem de eletronegatividade
Re: Ordem de eletronegatividade
miguelito3,1415926, essa lista foi criada como o propósito de facilitar a identificação dos elementos mais eletronegativos, alguns professores utilizam o EFEITO Mnemônico para decorar a lista, mas eu entendi o que você quis dizer, o problema é que pra destrinchar esse lista usando a metodologia CIENTÍFICA é um pouco complexo, pois para se AFERIR essa escala seria preciso levar em consideração 3 fatores (conforme indicado em VERMELHO no TEXTO abaixo):miguelito3,1415926 escreveu:Eletronegatividade é a tendência de um elemento de atrair pares eletrônicos ligantes para si em uma ligação química (ou, simplesmente, a tendência a atrair elétrons). Sabe-se que a seguinte lista determina a eletronegatividade de alguns dos principais elementos, em ordem decrescente:
F, O, N, Cl, Br, I, S, C, P, H.
Sei que a eletronegatividade depende do raio atômico (quanto menor o raio atômico, maior a eletronegatividade). Entretanto, como assimilo a lista citada sem precisar de decorebas ou dos raios atômicos dos elementos em questão ? Conheço as "setas" que indicam o sentido de crescimento da eletronegatividade nos elementos da tabela periódica, mas elas não me ajudaram muito a entender.
A atração que um par de elétrons de ligação sente por um determinado núcleo depende de:
- o número de prótons no núcleo;
- a distância do núcleo;
- a quantidade de blindagem por elétrons internos.
11.2: Electronegativity
Linus Pauling described electronegativity as “the power of an atom in a molecule to attract electrons to itself.”1 Basically, the electronegativity of an atom is a relative value of that atom's ability to attract election density toward itself when it bonds to another atom. The higher the electronegative of an element, the more that atom will attempt to pull electrons towards itself and away from any atom it bonds to. The main properties of an atom dictate it's electronegativity are it's atomic number as well as its atomic radius. The trend for electronegativity is to increase as you move from left to right and bottom to top across the periodic table. This means that the most electronegative atom is Fluorine and the least electronegative is Francium.
There are a few different 'types' of electronegativity which differ only in their definitions and the system by which they assign values for electronegativity. For example, there is Mulliken electronegativity which is defined as "the average of the ionization energy and electron affinity of an atom"3, which as we will see, differs slightly from Pauling's definition of electronegativity.
Pauling Electronegativity
Linus Pauling was the original scientist to describe the phenomena of electronegativity. By assigning a value of 4.0 to Fluorine (the most electronegative element), Pauling was able to set up relative values for all of the elements. This was when he first noticed the trend that the electronegativity of an atom was determined by it's position on the periodic table and that the electronegativity tended to increase as you moved left to right and bottom to top along the table. The range of values for Pauling's scale of electronegativity ranges from Fluorine (most electronegative = 4.0) to Francium (least electronegative = 0.7). Furthermore, if the electronegativity difference between two atoms is very large, then the bond type tends to be more ionic, however if the difference in electronegativity is small then it is a nonpolar covalent bond.
[size=16]Linus Pauling (1901-1994)
When he was nine, Pauling’s father died, and his mother tried to convince him to quit school to support the family. He did not quit school, but was later denied a high school degree, and had to work several jobs to put himself through college. Pauling would go on to become one of the most influential chemists of the century if not all time. He won two Nobel Prizes, one for chemistry in 1954 and one for peace in 1962.
[/size]
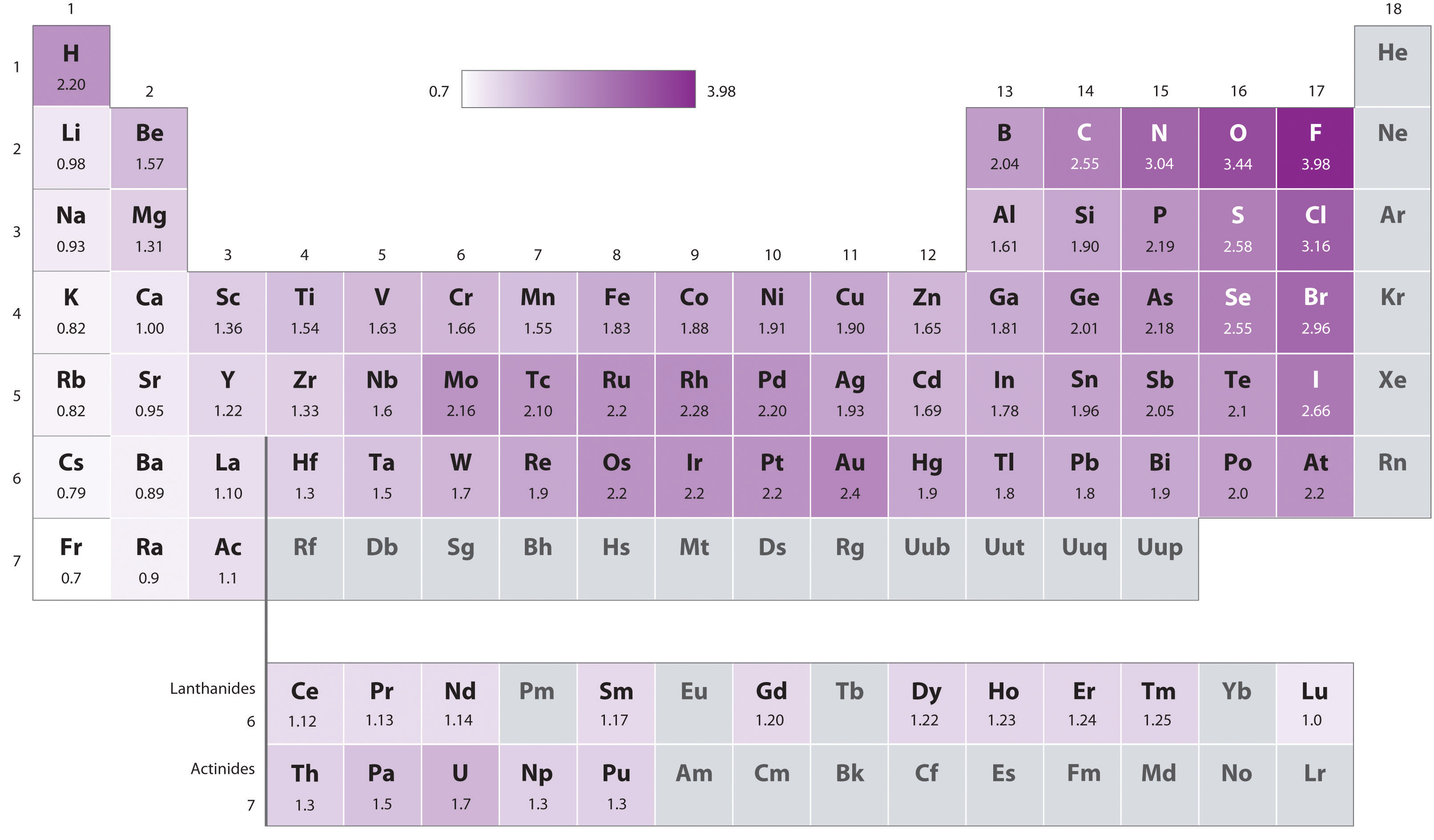
The attraction that a bonding pair of electrons feels for a particular nucleus depends on:
- the number of protons in the nucleus;
- the distance from the nucleus;
- the amount of screening by inner electrons.
Trends in electronegativity across a period
The positively charged protons in the nucleus attract the negatively charged electrons. As the number of protons in the nucleus increases, the electronegativity or attraction will increase. Therefore electronegativity increases from left to right in a row in the periodic table. This effect only holds true for a row in the periodic table because the attraction between charges falls off rapidly with distance. The chart shows electronegativities from sodium to chlorine (ignoring argon since it does not does not form bonds).
Why does electronegativity increase across a period? Consider sodium at the beginning of period 3 and chlorine at the end (ignoring the noble gas, argon). Think of sodium chloride as if it were covalently bonded.
Both sodium and chlorine have their bonding electrons in the 3-level. The electron pair is screened from both nuclei by the 1s, 2s and 2p electrons, but the chlorine nucleus has 6 more protons in it. It is no wonder the electron pair gets dragged so far towards the chlorine that ions are formed. Electronegativity increases across a period because the number of charges on the nucleus increases. That attracts the bonding pair of electrons more strongly.
Trends in electronegativity down a group
As you go down a group, electronegativity decreases. (If it increases up to fluorine, it must decrease as you go down.) The chart shows the patterns of electronegativity in Groups 1 and 7.
Why does electronegativity fall as you go down a group? As you go down a group, electronegativity decreases because the bonding pair of electrons is increasingly distant from the attraction of the nucleus. Consider the hydrogen fluoride and hydrogen chloride molecules:
The bonding pair is shielded from the fluorine's nucleus only by the 1s2 electrons. In the chlorine case it is shielded by all the 1s22s22p6 electrons. In each case there is a net pull from the center of the fluorine or chlorine of +7. But fluorine has the bonding pair in the 2-level rather than the 3-level as it is in chlorine. If it is closer to the nucleus, the attraction is greater.
Exercise
[ltr]11.2.111.2.1[/ltr]
Predict the order or increasing electronegativity from the following elements
- F, Li, C, O
- Te, Cl, S, Se
- Cs, At, Tl, I
Em relação ao CALCULO da CARGA NUCLEAR EFETIVA (que determina a a quantidade de blindagem por elétrons internos) você poderá obtê-la atraves desse link:
https://chem.libretexts.org/Bookshelves/General_Chemistry/Map%3A_Chemistry_-_The_Central_Science_(Brown_et_al.)/07%3A_Periodic_Properties_of_the_Elements/7.02%3A_Shielding_and_Effective_Nuclear_Charge
RESUMINDO: Num primeiro momento você pode até calcular a Zeff (CARGA NUCLEAR EFETIVA) para determinar a FILA DE ELETRONEGATIVIDADE, mas depois vai acabar optando pelo RECURSO MNEMÔNICO para decorar a referente fila.





Jigsaw- Monitor

- Mensagens : 572
Data de inscrição : 26/12/2020
Localização : São Paulo/SP
miguelito3,1415926 gosta desta mensagem
Página 1 de 1
Permissões neste sub-fórum
Não podes responder a tópicos|
|
|













